激光(guāng)顆粒計(jì)數(shù)器(qì)技(jì)術(shù)優勢:
1、兩次自(zì)動稀釋,适合濃度較高(gāo)的(de)樣品
2、符合21CFR法規軟件(jiàn)——符合cGMP要(yào)求;
3、現(xiàn)場(chǎng)校(xiào)準,無需返廠(chǎng);
4、模塊化(huà)設計(jì),便于升級及維護;
5、512通(tōng)道(dào),不(bù)放(fàng)過任何細微(wēi)顆粒;
6、符合美(měi)國(guó)藥典USP729,中國(guó)藥典CP等要(yào)求,且可('kě)自(zì)定義報(bào)告和(hé)标準;
7、集自(zì)動進樣、自(zì)動檢測、數(shù)據處理(lǐ)以及自(zì)動清洗等自(zì)動化(huà)功能(néng)與一(yγī)身(shēn);
512數(shù)據通(tōng)道(dào)
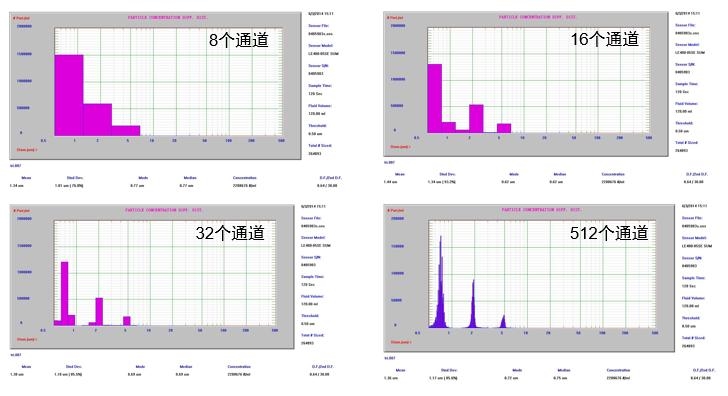
對(duì)于顆粒計(jì)數(shù)器(qì)來(lái)說(shuō),通(tōng)道(dào)數(shù)越多(duō),意味著(zhe)其在特定測量量程™內(nèi)劃分(fēn)的(de)區(qū)域越多(duō)。AccuSizer 780 顆粒計(jì)數(shù)器(qì)系列的(de)儀器(→qì)對(duì)于0.5μm - 400.0μm的(de)測量範圍按照(zhào)指數(shùφ)等級劃分(fēn)有(yǒu)512個(gè)通(tōng)道(dào),意味著(zhe)其在粒徑越小(xiǎo)處劃分(fēn)的(de)範圍越細,例:1.586μm-1.675&♠mu;m。這(zhè)樣做(zuò)的(de)優點是(shì)顯而易見(jiàn)的(de),一(yī)方面儀器(qì)實現(xiàn)了(l÷e)計(jì)數(shù)的(de)精準性,将測量的(de)結果作(zuò)細緻的(de)分(fēn)析,而不(bù)是(shì)将ε結果作(zuò)大(dà)緻的(de)分(fēn)類。另一(yī)方面,對(duì)于測量複雜(zá)體(tǐ)系和(hé)多(duō)組≠分(fēn)的(de)樣品,數(shù)據能(néng)很(hěn)好(hǎo)的(de)體(tǐ)現(xiàn)在結果圖譜及數(shù)≠據中。
如(rú)上(shàng)四張圖是(shì)同樣一(yī)個(gè)樣本在使用(yòng)不(bù)同通(tōng)道(dào)的(de)時(shí)候的(de)表現(xià€n),明(míng)顯可(kě)以看(kàn)出,使用(yòng)8、16、32個(gè)通(tōng)道(dào)的ε(de)時(shí)候,僅僅能(néng)判斷顆粒度在一(yī)個(gè)範圍內(nèi),不(bù)能(néng)<明(míng)确到(dào)底多(duō)大(dà)。而換用(yòng)512高(gāo)通(tōng)道(dào)後,粒徑大(dà)小(xiǎo)的(de)辨析度明(míng)顯增加,對(d↕uì)于峰值的(de)判斷更加清晰明(míng)了(le)。
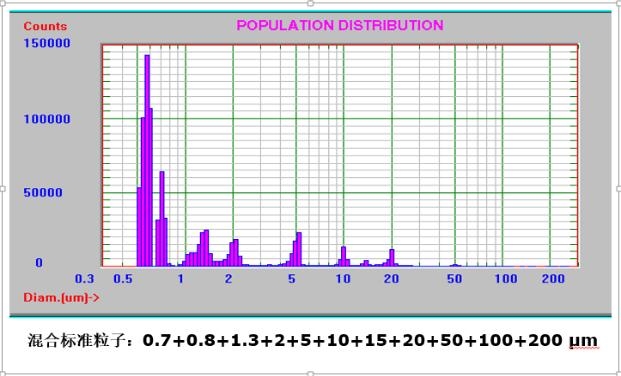
高(gāo)分(fēn)辨率
高(gāo)通(tōng)道(dào)的(de)優勢換來(lái)的(de)是(shì)高(gāo)分(fē↕n)辨率的(de)優勢。所謂分(fēn)辨率,在這(zhè)裡(lǐ)指的(de)是(shì)分(fēn)辨同一(yī)體(tǐ)系內(©nèi)不(bù)同粒徑大(dà)小(xiǎo)的(de)能(néng)力。得(de)益于超前的(de)設計(jì)理(lǐ)念和(hé)軟硬件(j↔iàn)組合,AccuSizer 780系列儀器(qì)除了(le)能(néng)夠呈現(xiàn)*不(bù)同于經典光(guāng)散射的(de)顆粒計(jì)數(shù)分(fēn)布外(wà'i),相(xiàng)對(duì)于經典的(de)電(diàn)阻法和(hé)光(guāng)阻法,具有(yǒu)更高(gāo)的(de)分(fēn)辨率和(hé)精準性。↓它不(bù)會(huì)錯(cuò)過任何“尾部” 大(dà)顆粒,而這(zhè)些(xiē)“尾¶部”大(dà)顆粒往往是(shì)決定産品好(hǎo)壞的(de)标準。
選配 21CFR Part 11法規軟件(jiàn)——符合cGMP要(yào)求
AccuSizer 780 A7000 APS不(bù)溶性微(wēi)粒檢測儀全系配備了(le)符合美(měi)國(guó)聯邦法規21章(zhāng)第11款(←21 CFR PART11)要(yào)求的(de)軟件(jiàn)。具有(yǒu)數(shù)據自(zì)動備份♠,審計(jì)追蹤,權限分(fēn)級,電(diàn)子(zǐ)簽名,可(kě)連接Lims系統等多(duō)項功能(néng)。
中國(guó)食品藥品監督管理(lǐ)局(NMPA)有(yǒu)政策趨勢将對(duì)醫(yī)藥研發企業(yè)實施規範的(de)GLP 管理(lǐ♣)。使用(yòng)符合21 CFR PART 11法規的(de)軟件(jiàn)更能(néng)符合現(xiàn)在GLP/GMP的(de)要(yào)求。
 QQ:
QQ: 郵箱:haitaozhang@labeach.cn
郵箱:haitaozhang@labeach.cn 傳真:
傳真: 地(dì)址:上(shàng)海(hǎi)市(shì)闵行(xíng)區(qū)滬闵路(lù)3988号A101
地(dì)址:上(shàng)海(hǎi)市(shì)闵行(xíng)區(qū)滬闵路(lù)3988号A101
